- Filtrar por
- Categorias
- Tags
- Autores
- Todos
- artigo científico
- comunicação médico-cientícica
- conteúdos ténicos-científicos
- desenvolvimento clínico de medicamentos
- desenvolvimento de medicamentos
- dossiê de desenvolvimento clínico de medicamentos
- elaboração de conteúdos técnicos-científicos
- estudo de bioequivalência
- patentes de medicamentos
- projetos de pesquisa
- protocolos de estudo de bioequivalência
- protocolos de pesquisa clinica
- redação científica
- redação de patentes de medicamentos
22/07/2022
ANVISA informou na quarta-feira (01/06) que entra em vigor a Resolução da Diretoria Colegiada (RDC) 687/2022, que dispõe sobre os critérios para a concessão ou renovação […]
Você gosta disso?0
15/07/2022
Com o objetivo de garantir a proteção dos direitos, segurança e bem estar dos participantes do ensaio clínico, bem como a precisão e confiabilidade dos dados […]
Você gosta disso?0
08/07/2022
Para a submissão de DDCM dever ser seguida a Seção II do Capítulo III da RDC nº 09/2015. Recomenda-se que toda a documentação seja submetida em […]
Você gosta disso?0
01/07/2022
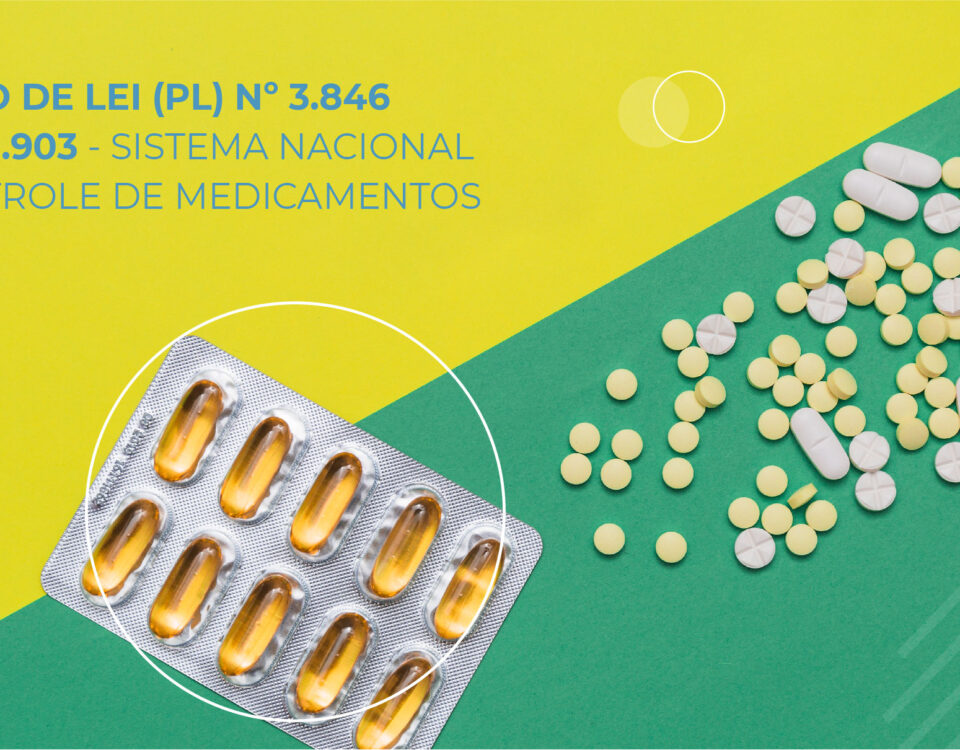
Lei nº 11.903/2009 criou o Sistema Nacional de Controle de Medicamentos (SNCM) com o objetivo de acompanhar os medicamentos em toda a cadeia produtiva, desde a […]
Você gosta disso?0
24/06/2022
A ANVISA informa que já estão disponíveis os códigos de assunto para o peticionamento conforme a RDC Nº 690/2022, que instituiu o piloto de implementação do Protocolo […]
Você gosta disso?0
17/06/2022
Com a finalidade de avaliar as etapas inerentes ao desenvolvimento de um medicamento experimental visando a obtenção de informações para subsidiar o registro ou alterações pós […]
Você gosta disso?0
10/06/2022
Com a publicação da Lei 14.338/2022 que altera a lei 11.903/2009 temos uma nova janela de tempo para a implantação da Rastreabilidade de Medicamentos no Brasil. Os responsáveis pelo […]
Você gosta disso?0
03/06/2022
A Diretoria Colegiada da ANVISA aprovou agora em 04/05, o uso emergencial do medicamento Molnupiravir, da empresa Merck Sharp & Dohme (MSD), para tratamento da Covid-19. […]
Você gosta disso?0
27/05/2022
A Resolução publicada no DOU em 30 de março de 2022 entrou em vigência na data de sua publicação alterando a RDC 430/2020 que dispõe sobre […]
Você gosta disso?0
20/05/2022
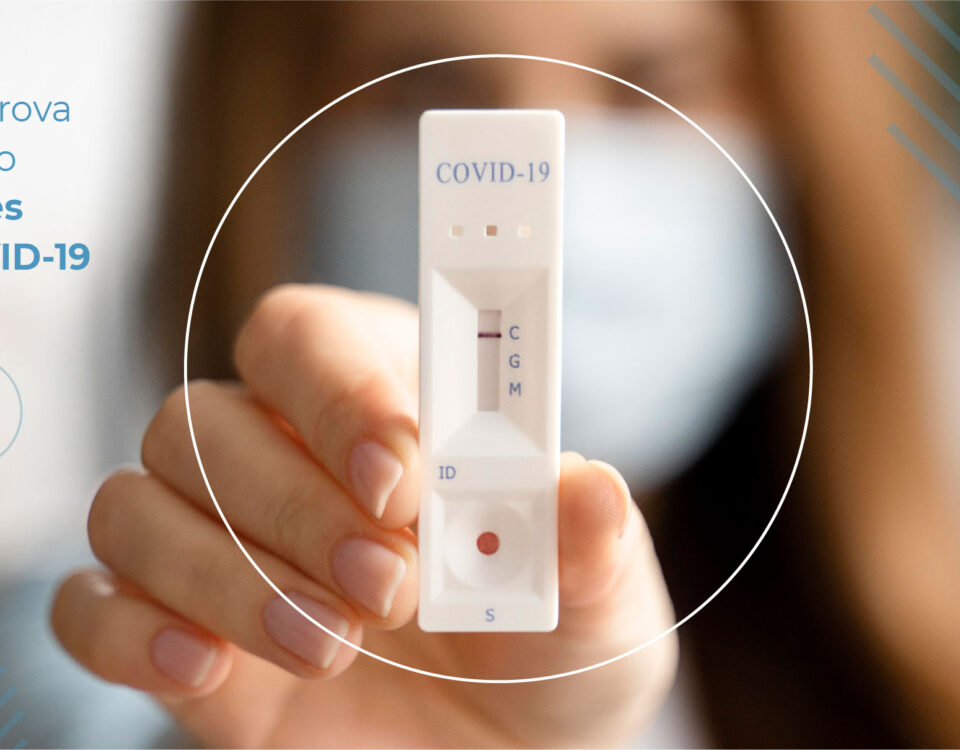
A ANVISA informa que aprovou o registro de cinco novos autotestes para Covid-19. As medidas foram publicadas no Diário Oficial da União (D.O.U.). Até o momento, […]
Você gosta disso?0
13/05/2022
A ANVISA se manteve listada entre as autoridades sanitárias que possuem status de equivalência com os controles da União Europeia para insumos farmacêuticos ativos (IFAs). Entre […]
Você gosta disso?0
06/05/2022
A ANVISA informa que aprovou o registro de cinco novos autotestes para Covid-19. As medidas foram publicadas no Diário Oficial da União (D.O.U.). Até o momento, […]
Você gosta disso?0